Hóa sinh thần kinh và hành vi
Tổ chức giải phẫu của não được bổ sung bởi một tổ chức hóa sinh thần kinh phức tạp không kém. Nhiều rối loạn hành vi phản ánh rối loạn chức năng sinh hóa và các biện pháp can thiệp hiệu quả nhất hiện có là về bản chất hóa sinh thần kinh. Những khiếm khuyết về hành vi thần kinh bắt nguồn từ các tổn thương khu trú ở vỏ não (ví dụ, thất ngôn, thất điều) đã hạn chế các phương pháp điều trị hóa sinh thần kinh có thể khắc phục được; rối loạn tâm thần kinh liên quan đến rối loạn chức năng hệ thống limbic thường có thể sửa đổi được thông qua các can thiệp hóa sinh thần kinh.
Có hai loại chất dẫn truyền não: 1) dẫn truyền truyền phát, hay chất dẫn truyền mở ra, có nguồn gốc từ các nhân dưới vỏ não và thân não, rồi đi tới các mục tiêu của não và 2) dẫn truyền cục bộ hoặc bên trong, bắt nguồn từ các neuron của não và truyền cục bộ đến các neuron lân cận hoặc bên cạnh. Các dẫn truyền truyền phát hoặc các enzyme tổng hợp của chúng phải được vận chuyển trong neuron với khoảng cách lớn, từ nhân dưới vỏ não đến các vùng xa, và do đó dễ bị gián đoạn, do đột quỵ, khối u và các quá trình khác. Theo quan điểm tiến hóa, các hệ dẫn truyền có tính bảo toàn cao và nhiều bộ dẫn truyền hoạt động cục bộ trong một số hệ thống thần kinh sẽ hoạt động như bộ truyền phát (đi xa hơn) ở các hệ thống khác. Các chất dẫn truyền thần kinh cổ điển đã phục vụ hoạt động giao tiếp thần kinh trong suốt 600 triệu năm tiến hóa (Rapoport 1990). Bảng 1 tóm tắt nguồn gốc và đích đến của các truyền phát đi ra.
BẢNG 1. Nguồn gốc và đích đến của các dẫn truyền thần kinh đi ra chủ yếu
| Chất dẫn truyền thần kinh | Nguồn | Đích |
| Acetylcholine | ||
| Hệ thống não trước- nền | Hạch nền và nhân dải chéo của Broca | Vỏ tân não, hồi hải mã, vùng dưới đồi, và hạch hạnh nhân |
| Hệ lưới | Cấu tạo lưới | Đồi thị |
| Dopamine | ||
| Hệ thống nhân đen- thể vân | Liềm đen | Nhân bèo và nhân đuôi |
| Hệ thống trung não- hồi viền | Vùng trần bụng | Nhân nằm, nhân vách, và hạch hạnh nhân |
| Hệ thống trung não- vỏ não | Vùng trần bụng | Thuỳ thái dương trong, thuỳ trán và vỏ não đai trước |
| Histamine | Vùng dưới đồi sau | Toàn bộ não |
| GABA | Vùng bất định | Vỏ tân não, hạch nền, và thân não |
| Nhân đuôi và nhân bèo | Cầu nhạt và liềm đen | |
| Cầu nhạt và liềm đen | Đồi thị | |
| Glutamate | Vỏ tân não | Nhân đuôi, nhân bèo, đồi thị, và nhân nằm |
| Nhân hạ đồi | Cầu nhạt | |
| Đồi thị | Vỏ tân não | |
| Hồi hải mã và giá đỡ | Vùng vách | |
| Vỏ não nội khứu | Hồi hải mã | |
| Norepinephrine | ||
| Đường lưng | Nhân lục | Đồi thị, hạch hạnh nhân, não trước nền, hồi hải mã, and vỏ tân não |
| Đường bụng | Nhân lục | Hồi hải mã cấu tạo lưới ở não giữa |
| Serotonin | Nhân đan | Toàn bộ não |
Tác dụng của chất dẫn truyền thần kinh được trung gian bởi các thụ thể mà chất dẫn truyền liên kết với, sau khi nó được giải phóng vào khe synap. Các thụ thể có thể nằm ở đầu tận cùng trước synap hoặc sau synap. Các thụ thể trước synap (autoreceptors) điều chỉnh sự tổng hợp hoặc giải phóng chất dẫn truyền thần kinh. Các thụ thể sau synap làm trung gian tác động của chất dẫn truyền thần kinh lên tế bào sau synap. Các cơ quan thụ cảm dị thể (các cơ quan thụ cảm dành cho chất dẫn truyền thần kinh không phải do neuron tạo ra) cũng điều chỉnh hoạt động của synap. Sự liên kết của chất dẫn truyền thần kinh với thụ thể dẫn đến việc mở kênh ion (thụ thể ionotropic) hoặc bắt đầu các dòng truyền tin thứ hai thông qua các protein liên kết (G) guanosine triphosphate (G) (thụ thể metabotropic). Chất dẫn truyền thần kinh được loại bỏ khỏi synap (trước hoặc sau khi liên kết với thụ thể) bằng enzyme phân hủy hoặc tái hấp thu tích cực vào đầu cuối trước synap nhờ protein vận chuyển có ái lực cao. Các hiệu ứng hành vi hiếm khi có thể được gán cho những thay đổi trong một hệ truyền dẫn duy nhất, nhưng một số hành vi bất thường có liên quan đến những thay đổi ảnh hưởng chủ yếu đến một loại bộ truyền. Bảng 2 trình bày các mối quan hệ truyền dẫn-hành vi chính hiện được xác định.
BẢNG 2. Thay đổi hành vi liên quan đến nhiễu loạn chất dẫn truyền
| Chất dẫn truyền thần kinh | Suy giảm chức năng | Tăng chức năng |
| Acetylcholine | Suy giảm trí nhớ, thờ ơ, mê sảng, hoang tưởng | Trầm cảm, hung hăng gây hấn |
| Dopamine | ||
| Motor function | Parkinsonism | Múa vờn, tics |
| Behavior | Suy giảm nhận thức (đặc biệt là không tập trung), thờ ơ, trầm cảm | Ảo giác, hoang tưởng, phấn chấn, hành vi ám ảnh nghi thức, rối loạn ưa chuộng tình dục |
| GABA | Co giật, lo âu | Mất trí nhớ, không phối hợp, an dịu |
| Glutamate | Suy giảm nhận thức (đặc biệt là mất nhớ), loạn thần, thờ ơ | S Co giật, kích thích nhiễm độc (excitotoxicity) |
| Norepinephrine | Suy giảm nhận thức (đặc biệt là không tập trung), trầm cảm, sa sút trí tuệ | Lo âu |
| Serotonin | Trầm cảm, lo âu, tự tử, hung hăng | Lú lẫn, hưng cảm nhẹ, cáu kỉnh, giật cơ |
Có một số nhân cholinergic riêng biệt truyền dẫn từ các vị trí dưới vỏ não đến não. Ở thân não, các nhân trần lưng bên (tegmental) và cuống cầu não cư trú trong hệ thống lưới và truyền dẫn qua con đường phía lưng đến đồi thị. Con đường này là thành phần thiết yếu của hệ thống kích hoạt hệ lưới đi lên (Arciniegas 2011; Nieuwenhuys 1985; Salmond và cộng sự, 2005). Các nhóm tế bào cholinergic của nền não trước là nguồn cung cấp acetylcholine chính cho não (Perry và cộng sự 1999; Salmond và cộng sự 2005; Selden và cộng sự 1998). Các truyền dẫn cholinergic ở nhân vách ngăn và nhánh đứng dọc của dải chéo của Broca dẫn qua trụ não đến hồi hải mã. Các tế bào nhánh ngang của dải chéo Broca thì cung cấp cho hành khứu. Các neuron cấu thành các nhân nền của Meynert thì phân thành nhiều bó riêng biệt tới hạch hạnh nhân, đến hồi đai và vỏ não trán ổ mắt, đến vỏ não thùy đảo và vỏ nắp (opercular), cũng như đến phần còn lại của vỏ não mới (Hình 1). Các sợi hướng đến đến nhân nền chủ yếu là từ các cấu trúc hệ viền ở vỏ não và dưới vỏ não, thiết lập các nhân nền như một sự chuyển mạch giữa các sợi hướng đến, của hệ limbic, và các sợi đi ra, đến vỏ não mới (Mesulam và Mufson 1984).
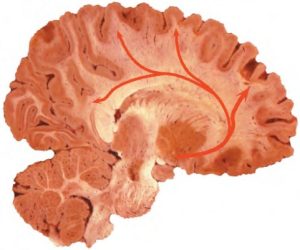 HÌNH 1. Các truyền dẫn cholinergic từ nhân nền (màu đỏ). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
HÌNH 1. Các truyền dẫn cholinergic từ nhân nền (màu đỏ). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
Chức năng cholinergic được trung gian bởi các thụ thể nicotinic (ionotropic) hoặc muscarinic (metabotropic). Các thụ thể muscarinic được phân loại về mặt dược lý là M1 (nằm trên neuron sau synap) hoặc M2 (nằm trên neuron trước synap) và có sự phân bố khác nhau khắp não. Hệ thống cholinergic làm trung gian cho loạt rộng rãi các hành vi. Sự gián đoạn chức năng cholinergic trung ương (ví dụ, thông qua việc sử dụng các chất ức chế thụ thể cholinergic như scopolamine) gây ra chứng mất nhớ (Bartus et al. 1982), và ngộ độc các hợp chất kháng cholinergic tạo ra mê sảng và hoang tưởng. Bệnh Alzheimer là một trong những rối loạn chính liên quan đến tình trạng thiếu cholinergic. Bệnh này gây tiêu nhân nền dẫn đến giảm tổng hợp choline acetyltransferase, enzyme tổng hợp acetylcholine; mất hoạt động tổng hợp dẫn đến gián đoạn chức năng cholinergic vỏ não (Katzman và Thal 1989). Bằng chứng ngày càng tăng cho thấy một số rối loạn tâm thần kinh của bệnh Alzheimer—ảo giác, thờ ơ, mất ức chế, hành vi không mục đích—là do thiếu hụt hệ cholinergic (Cummings và Kaufer 1996). Sự thiếu hụt cholinergic cũng là đặc điểm của bệnh sa sút trí tuệ thể Lewy và bệnh sa sút trí tuệ do bệnh Parkinson. Sự tăng hoạt động cholinergic đã được cho là có vai trò gây ra trầm cảm (Dilsaver và Coffman 1989), và ở một số loài, sự kích thích cholinergic của các cấu trúc hệ thống limbic tạo ra sự hung hăng (Valzelli 1981).
Có ba truyền dẫn dopaminergic chính từ thân não đến các bán cầu não: 1) dẫn truyền liềm đen- thể vân phát sinh từ phần đặc của liềm đen và đi đến nhân bèo và nhân đuôi, 2) dẫn truyền trung não- hệ viền (mesolimbic) bắt nguồn từ vùng mái bụng và truyền đến các cấu trúc của hệ viền (limbic), và 3) hệ thống trung não-vỏ não (mesocortical) bắt đầu ở vùng mái bụng và truyền tới các vùng trán và thái dương (Nieuwenhuys 1985) (Hình 2). Mục tiêu của truyền dẫn dopaminergic trung não- hệ viền (mesolimbic) bao gồm nhân nằm (accumbens), nhân vách ngăn và hạch hạnh nhân. Các truyền dẫn trung não-vỏ não kết thúc chủ yếu ở thùy trán trong, thùy thái dương trong và vùng đai trước. Các truyền dẫn kém mạnh mẽ hơn được phân phối đến vỏ não mới.
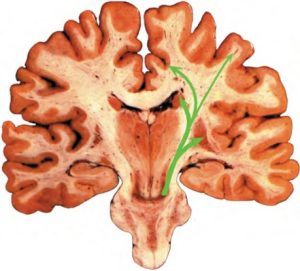 HÌNH 2. Các truyền dẫn dopaminergic; nhân đen- thể vân và trung não-vỏ não, phát sinh tương ứng từ vùng liềm đen và vùng mái bụng (màu xanh lá cây). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
HÌNH 2. Các truyền dẫn dopaminergic; nhân đen- thể vân và trung não-vỏ não, phát sinh tương ứng từ vùng liềm đen và vùng mái bụng (màu xanh lá cây). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
Chức năng Dopaminergic được trung gian bởi các thụ thể chuyển hóa (metabotropic) có thể được phân loại về mặt dược lý là giống D1 (kích thích adenosine monophosphate tuần hoàn [cAMP]) hoặc giống D2 (ức chế cAMP). Những thụ thể này có sự phân bố khác nhau khắp não. Các thụ thể D2 bị chặn bởi thuốc an thần kinh, và có thể các phân nhóm của thụ thể D2 điều hòa một cách khác nhau các tác động lên vận động và tâm thần của thuốc dopaminergic.
Dopamine đóng một vai trò quan trọng trong các chức năng và hành vi vận động. Thiếu hoặc phong tỏa Dopamine dẫn đến bệnh Parkinson; sự dư thừa dopamine sẽ tạo ra múa giật, rối loạn chuỗi động (dyskinesia) hoặc giật cơ. Về mặt hành vi, sự thiếu hụt dopamine ít nhất gây ra suy giảm nhận thức nhẹ và có thể góp phần gây ra trầm cảm thường đi kèm với bệnh Parkinson và các hội chứng Parkinson khác. Sự dư thừa Dopamine dẫn đến rối loạn loạn thần, hưng phấn hoặc hưng cảm nhẹ và lú lẫn. Sự gia tăng hoạt động của Dopamine có thể góp phần vào sinh lý bệnh của tâm thần phân liệt, hành vi ám ảnh cưỡng chế, lo âu và một số hành vi rối loạn ưa chuộng (paraphilic) (Cummings 1985, 1991).
Nhân lục (locus coeruleus) và các nhân lân cận tạo thành nguồn gốc của hệ thống truyền dẫn noradrenergic. Một bó noradrenergic lưng chạy từ thân não sau đến vách ngăn, đồi thị, hạch hạnh nhân, nền não, hồi hải mã và vỏ não mới (Nieuwenhuys 1985) (Hình 3). Một bó noradrenergic ở bụng chiếu tới vùng dưới đồi và hình thành lưới não giữa. Chức năng adrenergic được trung gian bởi các thụ thể chuyển hóa (metabotropic) có thể được phân loại về mặt dược lý là thụ thể α (ức chế cAMP) hoặc β (kích thích cAMP). Các thụ thể α-Adrenergic có thể được phân loại thêm thành α1 hoặc α2; cái trước được định vị ở vị trí sau synap và cái sau ở vị trí trước synap và sau synap. Những thụ thể này có sự phân bố khác nhau khắp não. Điều trị trầm cảm hiệu quả có liên quan đến việc giảm số lượng (điều hòa giảm) các thụ thể β-adrenergic. Suy giảm chức năng noradrenergic có liên quan đến trầm cảm, sa sút trí tuệ, giảm sự cảnh báo (alertness) và tập trung (Agid et al. 1987). Hoạt động noradrenergic tăng lên có liên quan đến lo âu (Lechin và cộng sự 1989).
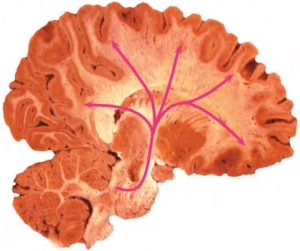 HÌNH 3. Các truyền dẫn noradrenergic từ nhân lục (locus coeruleus) (màu hồng). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
HÌNH 3. Các truyền dẫn noradrenergic từ nhân lục (locus coeruleus) (màu hồng). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
Các tế bào thần kinh tiết serotonin hầu như chỉ nằm ở nhân đan (raphe) trong và cận trong của hành tủy, cầu não và não giữa (Hình 4). Truyền dẫn của các neuron serotonergic này là một hệ thống sợi phức tạp, có nhiều nhánh, bao trùm gần như toàn bộ hệ thống thần kinh trung ương (Nieuwenhuys 1985). Chức năng serotonin được trung gian bởi nhiều thụ thể chuyển hóa (metabotropic) (ví dụ, 5-HT1, 5-HT2, 5-HT4) và ở mức độ thấp hơn bởi các thụ thể ion (ionotropic) (ví dụ, 5-HT3). Những thụ thể này có sự phân bố khác nhau khắp não. Người ta đưa ra giả thuyết rằng sự thiếu hụt serotonin đóng vai trò chính trong tự tử, trầm cảm, lo âu và hung hăng (Agid và cộng sự 1987), và việc dư thừa serotonin trong não có thể gây ra lú lẫn, hưng cảm nhẹ, kích động và giật cơ (Isbister và Buckley 2005). Các thụ thể 5-HT2A có liên quan đến sinh lý bệnh của rối loạn loạn thần.
HÌNH 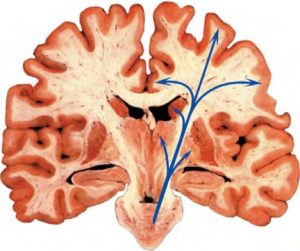 4. Các truyền dẫn serotonin (màu xanh). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
4. Các truyền dẫn serotonin (màu xanh). Nguồn. Hình ảnh được cung cấp bởi M. Mega và Phòng thí nghiệm hình ảnh thần kinh của UCLA.
Axit γ-Aminobutyric (GABA) là một chất dẫn truyền thần kinh ức chế có trong cả hệ thống truyền dẫn và mạch thần kinh cục bộ. Hệ thống truyền dẫn GABA chính bắt đầu ở vùng vô danh (zona incerta) và dẫn truyền ở hai bên tới toàn bộ vỏ não mới, hạch nền và thân não (Lin và cộng sự 1990). Ở các vùng dưới vỏ não, một hệ thống truyền dẫn bắt nguồn từ nhân đuôi và nhân bèo rồi dẫn tới các cầu nhạt và liềm đen, và một hệ thống khác bắt đầu ở các cầu nhạt và liềm đen với các phần dẫn truyền tới đồi thị (Alexander và Crutcher 1990; Nieuwenhuys 1985). Các neuron mạch cục bộ sử dụng GABA được tìm thấy trong nhân đan (raphe), nhân lưới của đồi thị và hạch nền. Các neuron mạch cục bộ của vỏ não cũng sử dụng GABA làm chất dẫn truyền thần kinh chính (Rapoport 1990). Chức năng GABA được trung gian bởi các thụ thể ionotropic (GABA-A) và metabotropic (GABA-B), các thụ thể trước đây được tâm thần kinh học đặc biệt quan tâm vì chúng chứa các vị trí gắn kết với rượu, thuốc chống co giật và các loại thuốc benzodiazepin. Những thụ thể này có sự phân bố khác nhau khắp não. Nồng độ GABA giảm trong hạch nền của bệnh nhân mắc bệnh Huntington và sự thiếu hụt GABA có thể góp phần gây ra sa sút trí tuệ, rối loạn khí sắc, rối loạn ám ảnh nghi thức và rối loạn loạn thần, xảy ra với tần suất ngày càng tăng trong bệnh lý này (Morris 1991).
Glutamate là một chất dẫn truyền thần kinh kích thích, được sử dụng trong sự truyền dẫn rộng rãi từ vỏ não mới đến nhân đuôi, nhân bèo và nhân nằm/ giường (accumbens) cùng bên. Glutamate là chất dẫn truyền thần kinh chính của các truyền dẫn từ vỏ não đến đồi thị, từ đồi thị đến vỏ não và từ vùng vỏ não này sang vùng vỏ não khác. Các neuron glutamatergic cũng dẫn truyền từ nhân dưới đồi đến nhân cầu nhạt. Chức năng của glutamate trong một số truyền dẫn liên quan đến hồi hải mã, bao gồm cả con đường xuyên qua từ vỏ não nội khứu đến hồi hải mã và các con đường bắt nguồn từ vùng hải mã và lân cận bệ đỡ (subiculum) rồi dẫn đến vùng vách ngăn (Alexander và Crutcher 1990; Nieuwenhuys 1985). Chức năng glutamatergic được trung gian bởi các thụ thể ionotropic và metabotropic, với các phân nhóm trước đây (ví dụ, thụ thể N-methyl-D-aspartate (NMDA)) có liên quan đến việc học tập, độc tính kích thích và tác dụng kích thích tâm thần của phencyclidine (PCP). Những thụ thể này có sự phân bố khác nhau khắp não. Hậu quả hành vi của sự thay đổi chức năng glutamate là rất đáng kể. Sự đối kháng của các thụ thể NMDA do PCP hoặc ketamine gây ra là một mô hình dược lý hữu ích cho tâm thần phân liệt, ở chỗ, nó dẫn đến các triệu chứng dương tính (ví dụ: ảo giác, hoang tưởng, rối loạn kiểm soát hành vi), các triệu chứng âm tính (ví dụ: chứng mất ngủ, mất cảm giác hưng phấn, mất trí nhớ) và rối loạn nhận thức. sự suy yếu của tình trạng này (Javitt 2007). Các chất đối kháng NMDA không cạnh tranh như memantine cải thiện nhận thức trong bệnh Alzheimer, ngụ ý vai trò của hệ thống truyền này trong nhận thức. Sự dư thừa glutamatergic có liên quan đến sự hình thành phát và triển của các cơn động kinh (ictogen) nói chung và đặc biệt là bệnh động kinh thùy thái dương giữa (mesial) (Eid et al. 2008).
Orexin được phát hiện gần như đồng thời vào năm 1998 bởi hai nhóm nghiên cứu độc lập, đang nghiên cứu hệ thần kinh trung ương của loài gặm nhấm (de Lecea và cộng sự 1998; Sakurai và cộng sự 1998). Một nhóm (Sakurai và cộng sự 1998) đặt tên nó là orexin, từ orexis, có nghĩa là “thèm ăn” trong tiếng Hy Lạp; nhóm còn lại (de Lecea và cộng sự 1998) đặt tên cho nó là hypocretin, vì nó được sản xuất ở vùng dưới đồi và có chút giống với secretin. Mặc dù thường được sử dụng thay thế cho nhau, nhưng hypocretin hiện được sử dụng để chỉ các sản phẩm tiền chất protein của gen HCRT trên nhiễm sắc thể 17 (tức là, protein tiền neuropeptide hypocretin tạo ra hypocretin-1 và -2), và orexin đề cập đến các peptide thần kinh kích thích trưởng thành (orexin-A và B). Có khoảng 70.000 tế bào thần kinh sản xuất orexin ở vùng dưới đồi sau và vùng dưới đồi bên. Những neuron này truyền dẫn tới các nhân của thân não, gian não và nền não trước, liên quan đến việc điều biến trạng thái tỉnh táo. Thông qua sự điều biến này, orexin tạo điều kiện tích hợp các ảnh hưởng về chuyển hóa, nhịp sinh học và giấc ngủ theo cách điều khiển sự tỉnh táo và/hoặc giấc ngủ.
Nhân củ núm vú (tuberomammillary TMN), nằm ở vùng dưới đồi, là nơi duy nhất tổng hợp histamine thần kinh trong não động vật có vú trưởng thành và là nguồn dẫn truyền histaminergic đến tất cả các bộ phận chính của não (Nieuwenhuys 1985). Các tế bào thần kinh histaminergic của TMN có kiểu truyền đi có chọn lọc nhất trong số tất cả các neuron đã biết. Chúng hoạt động trong chu kỳ “đánh thức”, phát ra ở tần số khoảng 2 Hz; trong khi ngủ sóng chậm, tốc độ kích hoạt này giảm xuống 0,5 Hz; những neuron này ngừng hoạt động hoàn toàn trong giấc ngủ REM. Sự giải phóng histamine từ các neuron TMN (ví dụ, bởi orexin) thúc đẩy sự tỉnh táo bằng cách kích hoạt (ít nhất) các neuron cholinergic ở nền não trước, neuron nhân đan (raphe) serotonergic và neuron đồi thị thông qua thụ thể H1. Do đó, thuốc đối kháng thụ thể H1 vượt qua hàng rào máu não có tác dụng an thần (giảm hưng phấn). Thuốc đối kháng thụ thể H3 (hoạt động như chất chủ vận nghịch đảo) làm tăng sự tỉnh táo bằng cách thúc đẩy giải phóng histamine và các chất dẫn truyền thần kinh khác.
Glycine là một chất dẫn truyền ức chế có thể hoạt động trong các tế bào thần kinh mạch cục bộ ở liềm đen, nhân đuôi và nhân bèo. Chất P hiện diện trong đường truyền từ nhân đuôi và nhân bèo đến liềm đen, còn các neuron chứa enkephalin thì dẫn từ nhân đuôi và nhân bèo đến nhân cầu nhạt (Alexander và Crutcher 1990; Nieuwenhuys 1985). Các neuron peptide ở ruột do dây X kích hoạt, có bản chất của vỏ não, và tham gia vào các mạch thần kinh cục bộ (Nieuwenhuys 1985).
Phần kết luận
Bộ não bao gồm một vùng trung gian làm trung gian cho các chức năng cảnh thức và duy trì sự sống cơ bản, chẳng hạn như hô hấp, tiêu hóa, tuần hoàn và chức năng thần kinh nội tiết; vùng cận trong-limbic làm trung gian cho chức năng ngoại tháp và nhiều khía cạnh của trải nghiệm cảm xúc; còn vùng thượng limbic-tân vỏ não làm trung gian cho các chức năng nhận thức công cụ như ngôn ngữ và vận hành (praxis). Tổn thương vùng thượng limbic-tân vỏ não có liên quan đến các hội chứng khuyết thiếu hành vi thần kinh, chẳng hạn như thất ngôn (aphasia) và thất vận hành (apraxia); rối loạn chức năng của vùng cận trong-limbic tương quan với các rối loạn tâm thần kinh, bao gồm rối loạn khí sắc, rối loạn loạn thần, lo âu và rối loạn ám ảnh nghi thức. Trong mỗi vùng, rối loạn hành vi có liên quan đến rối loạn chức năng của một hoặc nhiều chất dẫn truyền thần kinh. Mô hình giải phẫu thần kinh hành vi này cung cấp một khuôn khổ toàn diện để hiểu các mối quan hệ giữa não và hành vi cũng như sự xáo trộn của những mối quan hệ đó được quan sát thấy trong thực hành lâm sàng.